中学3年理科。原子とイオンのつくりについて学習します。
- レベル★★☆☆
- 重要度★★★★
- ポイント:電子を失うと陽イオン!受けとると陰イオン!
授業用まとめプリントは下記リンクからダウンロード!
授業用まとめプリント「原子とイオン」
原子とイオン
物質を構成する最小の粒を原子といいました。今日はまず、原子のつくりを詳しくみていきます。どのような粒子で原子ができているのかを覚えましょう。
次に、この原子が電気を帯びたものであるイオンを学習します。原子はイオンになることでさまざまな化学変化を起こせるようになります。
ここは、これから学習を進めるうえでの土台となるので、しっかりと覚えてから次の学習内容に入るようにしましょう。
原子のつくり
まずは原子です。原子は物質を構成する最小の粒で、物質の性質を示さない粒でした。それ以上分解することができません。この原子をもっと詳しくみていきます。下の図を見てください。
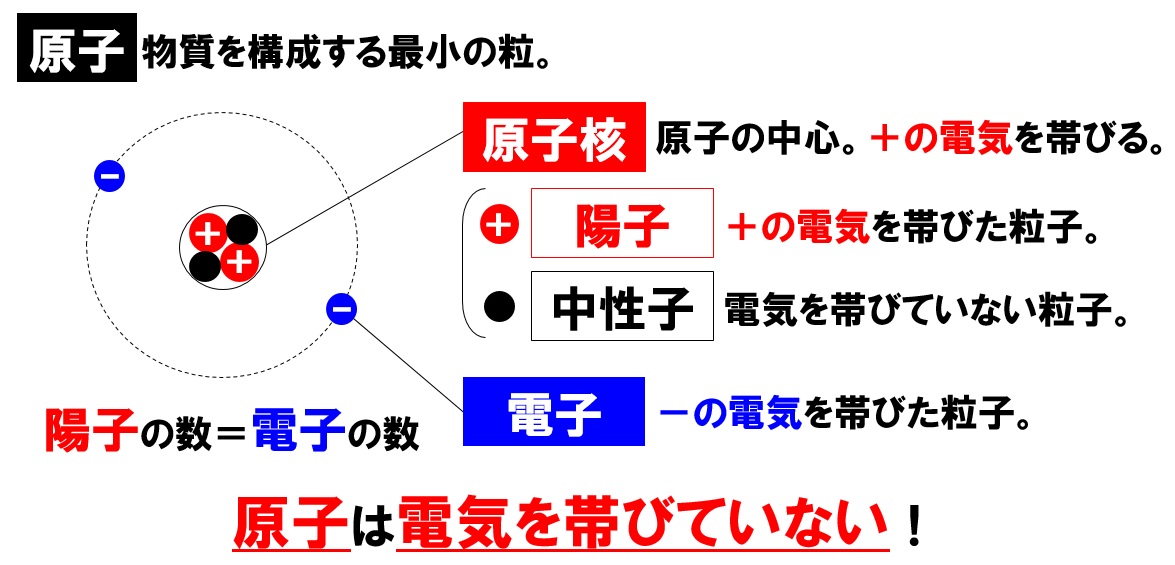
原子の中心には、原子核があります。原子核の中には、+の電気を帯びた陽子という粒と、電気を帯びていない中性子という粒が入っています。原子ごとにこの陽子と中性子の数は異なります。
その原子核のまわりをハエのように飛び回っているのが、ーの電気を帯びた粒子である電子です。ここで大事な決まりがあります。原子では、原子核の中にある陽子の数と、原子核のまわりを飛んでいる電子の数が同じになっています。
陽子は+の電気を帯びていて、電子はーの電気を帯びています。その数が同じということは、原子全体では電気を帯びていない状態になっているのです。
原子のポイント
- 原子核には+の電気を帯びた陽子と、電気を帯びていない中性子がある。
- 原子核のまわりをーの電気を帯びた電子が飛んでいる。
- 原子では、陽子と電子の数が同じになっており、原子全体では電気を帯びていない。
次の文は、原子のつくりについてまとめたものである。これについて以下の各問に答えよ。
解答①+ ②電子 ③陽子 ④中性子
イオンのでき方
原子が電気をおびたものをイオンといいます。では、どのようにして原子が電気を帯びイオンに変化するのでしょうか。それは電子のやり取りが原因になっています。
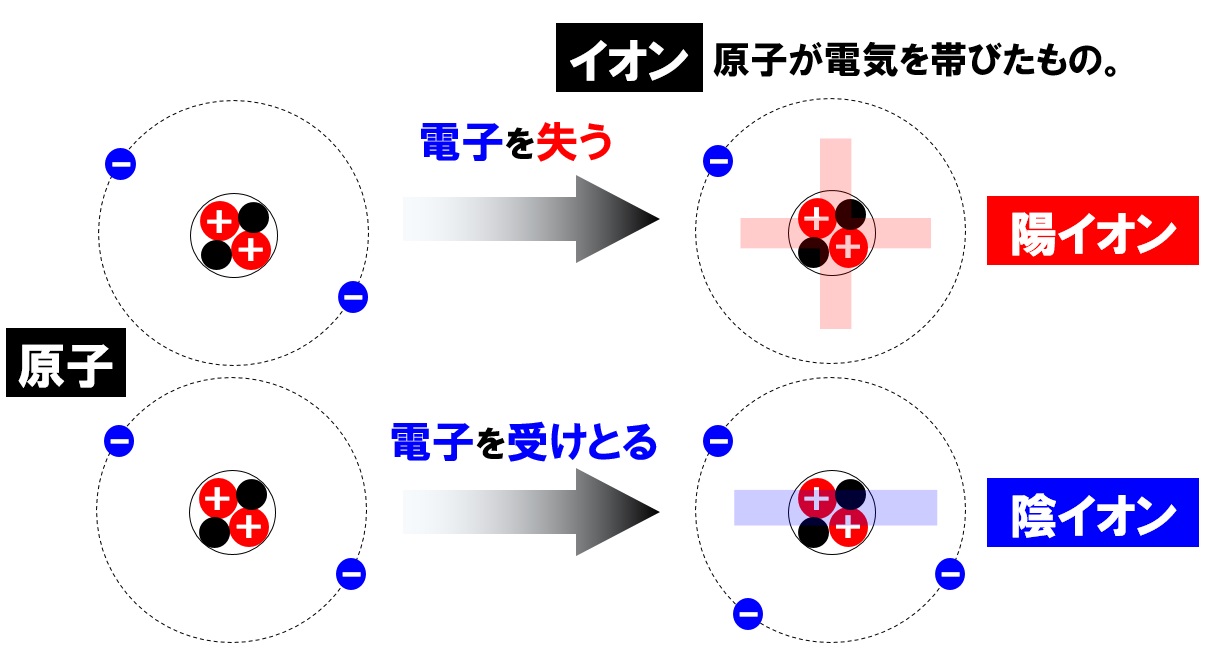
陽イオン
原子が+の電気を帯びたものを陽イオンといいます。陽イオンは、原子が電子を失ってできます。原子では陽子と電子の数が同じになっていました。この状態からーの電気を帯びた電子を失うのですから、陽子の数の方が多くなり原子は全体的に+の電気を帯びます。これが陽イオンです。
陰イオン
原子がーの電気を帯びたものを陰イオンといいます。陰イオンは、原子が電子を受けとってできます。原子では陽子と電子の数が同じになっていました。この状態からーの電気を帯びた電子を受けとるのですから、電子の数の方が多くなり原子は全体的にーの電気を帯びます。これが陰イオンです。
イオンのポイント
- 原子が電子を失うと陽イオンになる。
- 原子が電子を受けとると陰イオンになる。
次の文は、イオンのでき方についてまとめたものである。これについて以下の各問に答えよ。
解答①イオン ②陽イオン ③陰イオン

コメント